Chemiker der Universität Münster entwickeln Synthesemethode für den regioselektiven Einbau der biologisch relevanten Difluormethylgruppe in Pyridine
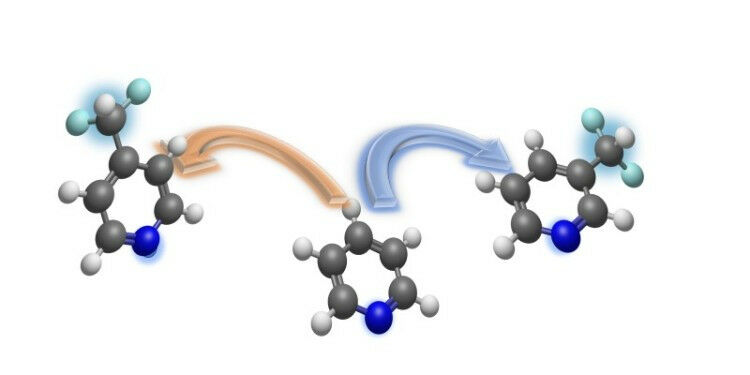
Pyridin ist in der Pharmaund agrochemischen Industrie ein wichtiger Baustein zur Herstellung biologisch aktiver Substanzen. Pyridin und seine Abkömmlinge enthalten Ringe mit fünf Kohlenstoffatomen und einem Stickstoffatom. Die Difluormethylgruppe lässt sich mit der neuen Methode entweder an der Meta-Position (zwei Atome vom Stickstoff entfernt) oder an der Para-Position (drei Atome vom Stickstoff entfernt) einbauen. Das ist für Chemiker deshalb interessant, weil die regioselektive Difluormethylierung von Pyridinen als Herausforderung gilt. Methoden für eine regioselektive Metaund Para-Difluormethylierung, die sich zwischen den beiden Positionen umschalten lässt, waren zuvor unbekannt. ,,Unsere Studie löst das Problem der direkten Difluormethylierung des Pyridinrings an der besonders schwer zugänglichen Meta-Position in komplexen Verbindungen", betont Armido Studer.
Da Pyridine eher reaktionsträge Verbindungen sind, wenden die Chemiker eine Strategie der temporären Dearomatisierung an. Die dearomatisierten aktiveren Zwischenprodukte reagieren mit Reagenzien, die Difluormethylgruppen beinhalten, und bilden schließlich die chemisch funktionalisierten Pyridine. Diese Methode ist auch für die Difluormethylierung von pyridinhaltigen Arzneimitteln am Ende der Synthesesequenz geeignet - die Pyridinabkömmlinge lassen sich also leicht umbauen, statt aufwändig neu aufgebaut werden zu müssen.
,,Unsere Methode ist praktikabel und lässt sich mit günstigen, im Handel erhältlichen Reagenzien durchführen. Das sollte unser Verfahren für das Design von Medikamenten relevant machen", unterstreicht Postdoktorand Dr. Pengwei Xu. ,,Wir gehen davon aus, dass unser Ansatz in der pharmazeutischen und agrochemischen Industrie Anwendung finden wird."
Die Deutsche Forschungsgemeinschaft (DFG), die Alexander-von-Humboldt-Stiftung und der China Scholarship Council unterstützten die Arbeiten finanziell.
Originalveröffentlichung:
Pengwei Xu, Zhe Wang, Shu-Min Guo and Armido Studer (2024): Introduction of the difluoromethyl group at the meta- or para-position of pyridines through regioselectivity switch. Nature Communications; DOI: 10.1038/s41467’024 -48383-1